Namen: Dorothea Schwendich, Mark Aland , Luca Marie Brenzel 2019-04
Die nicht-kompetitive Hemmung
Gifte, wie zum Beispiel Schwermetalle können Enzyme "vergiften" und sie dauerhaft unwirksam machen.
Positiv geladene Schwermetall-Ionen als nicht kompetitiver Inhibitor binden sich zufällig an negative Stellen der Protein-Aminosäurenkette. Beispiele für Schwermetalle sind: Blei (Pb), Quecksilber (Hg), Cadmium (Cd), Zinn (Sn) uvm.
Es kommt zu einer Verformung der Sekundär- und Tertiärstruktur aufgrund der großen Form des Schwermetall-Ions, welche in das Protein eindringt.
Daraus folgt, dass das aktive Zentrum verändert wird ,so dass das Substrat nicht mehr in der Lage ist in das Enzym zu gelangen (Enzym-Substrat-Komplex kann nicht gebildet werden).
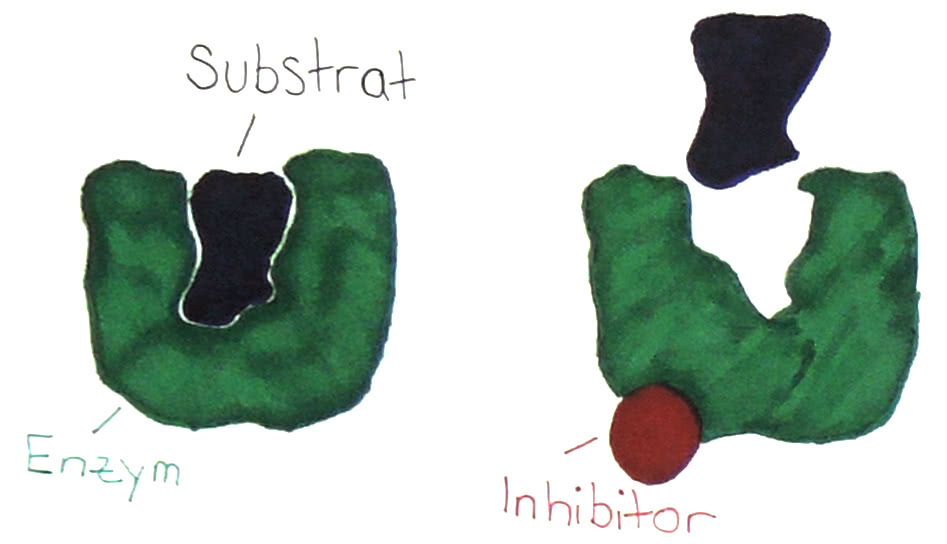
Aufgrund der sehr starken Bindung (oft durch einen Ionenbindung zwischen dem positiven Metallion und einer negativen Carboxylgruppe eines AS-Restes), ist es schwer das Schwermetall wieder zu lösen (dauerhafte Bindung).
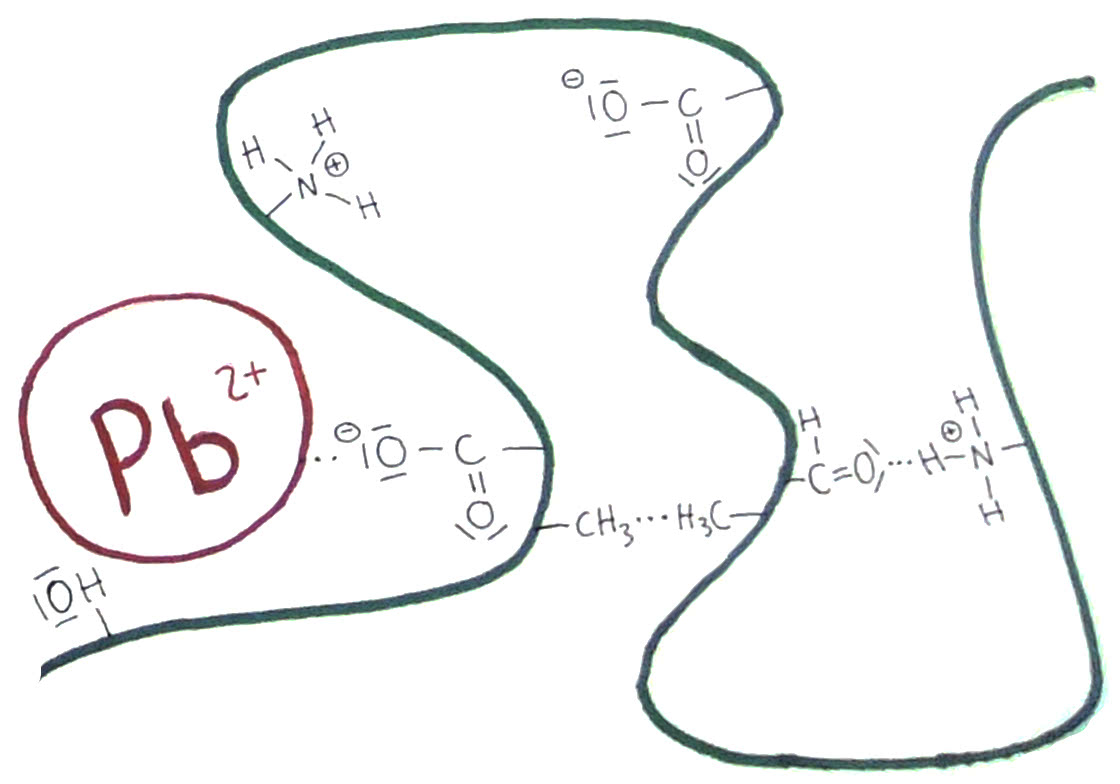
Da diese Bindung in der Regel nicht am aktiven Zentrum geschieht, kann eine Erhöhung der Substratkonzentration die Hemmung nicht verringern! Demnach handelt es sich um eine irreversible Hemmung => nicht-kompetitiv!

Die nicht komepetitive Hemmung (Klicken zur Vergrößerung)
Ursachen der Nicht-kompetitiven Hemmung:
Direkte Aufnahme des Schwermetalls überwiegend durch Nahrung:
• Pilzverzehr
• Bleihaltiges Trinkwasser
• Metallimplantate überwiegend in der Zahnmedizin
• Verunreinigte Luft durch Abgase
Folgen:
• Bauchkrämpfe
• Kopf- und Gliederschmerzen
• Schlaflosigkeit
• Zittern
• Lähmungserscheinungen
