Name: Jonas Reinhart, 05.06.2013
Citratzyklus
Im Verlauf der Zellatmung wird Glucose als energiereiches Produkt der Fotosynthese (oder mit der Nahrung aufgebommen) in die beiden energiearmen anorganischen Stoffe CO2 und H2O, unter Bindung der dadurch freiwerdenden Energie an die Reduktionsäquivalente FADH2 und NADH + H+,z erlegt. Dem Citratzyklus voraus geht die Glycolyse, welche aus einem Glucosemolekül zwei BTS (Brenztraubensäure) -Moleküle dem Zyklus zur Verfügung stellt und dabei 2 ATP und NADH + H+ herstellt.
Durch ein Carrier-Transport-Protein an der Mitochondrienmembran gelangen die 2 BTS-Moleküle aus dem Cytoplasma durch den perimitochondrialen Raum in die Mitochondrienmatrix. Dort lagert sich die Brenztraubensäure an einen Multienzymkomplex (Pyruvat-Dehydrogenase-Komplex) an, der die Reaktion der oxidativen Decarboxylierung katalysiert.
Oxidative Decarboxylierung:
Am C3-Körper der BTS erfolgt eine Abspaltung von Kohlenstoffdioxid aus der Carboxylgruppe und weiterhin wird das verbleibende Ion durch Elektronenentzug oxidiert. Die entzogenen Elektronen gelangen mit 2 Protonen auf NAD+ , wodurch es zu NADH + H+ reduziert wird. Der durch die Decarboxylierung entstandene C2-Körper (Acetat) wird als Acetylgruppe auf das Coenzym A übertragen, sodass diese nun aktiviert in den eigentlichen Citratzyklus eingebracht werden kann.
2 BTS + 2 NAD+ + 2 CoA-SH + 2 H+ → 2 Acetyl-CoA + 2 NADH +2 H+ + 2 CO2
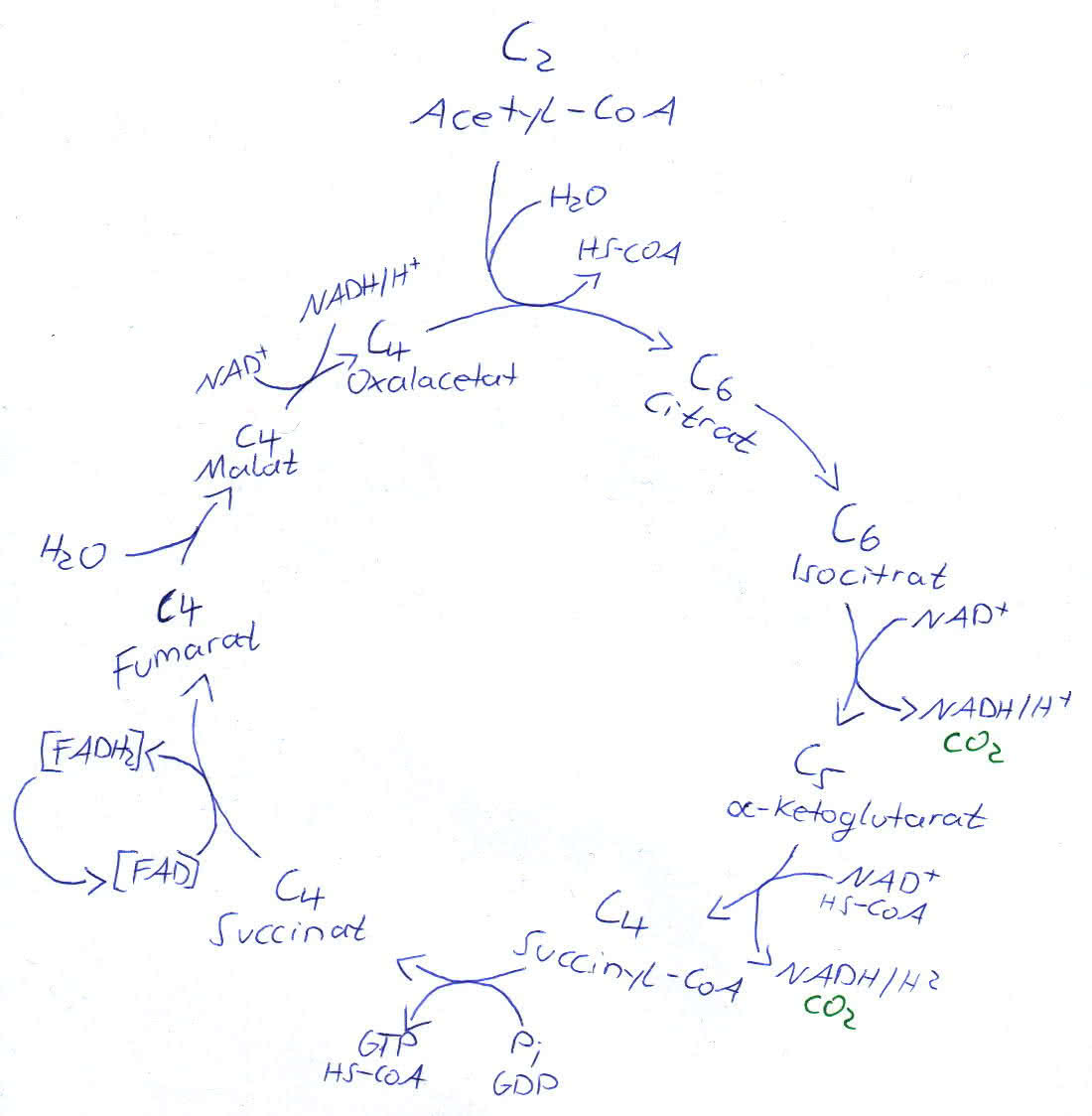
Citratzyklus:
Unter Verwendung von H2O und unter Abspaltung von CoA wird der C2-Körper an den C4-Körper des Oxalacetats, dem Säurerest der Oxalessigsäure, gebunden, sodass als Reaktionsprodukt Citrat als C6-Körper entsteht. Diese reaktion wird durch das Enzym Citrat-Synthase katalysiert. Was folgt, ist die Umwandlung in die isomere Verbindung Isocitrat durch die Aconitat-Hydratase und danach die Reaktion zu α-Ketoglutarat (C5-Körper) durch das Enzym Isocitrat-Dehydrogenase. Während des zuletzt genannten Schrittes wird CO2 abgespalten und NAD+ zu NADH + H+ reduziert.
Eine weitere oxidative Decarboxylierung durch den Multienzymkomplex α-Ketoglutarat-Dehydrogenase-K. führt zur fortführenden Abspaltung von CO2 und zur Reduktion von NAD+. Dabei wird das entstandene Produkt mit dem Coenzym A verknüpt,wodurch Succinyl - CoA entsteht, ein C4-Körper. Dadurch, dass das CoA durch eine Phosphatgruppe ersetzt wird, kommt es zur Phosphorylierung, die Phosphatgruppe wird auf Adenosindiphosphat übertragen.
Es entsteht ATP, unter zusätzlicher Verwendung von H2O kommt es damit zur Bildung von Succinat, dem Anion der Bernsteinsäure, durch die Succinyl-CoA-Synthetase.
Als weiterer Schritt folgt die Reduktion von Flavinadenindinucleotid (FAD) zu FADH2 es bildet sich Fumarat, Säurerest der Fumarsäure mithilfe des Katalysators Succinat-Dehydrogenase. Im Verlauf der Regenertaion des Akzeptors des aktivierten Acetyl-Coenzym A, dem Oxalacetat, wird nun duch die Fumarat-Hydratase mithilfe von H2O Malat,das Anion der Äpfelsäure hergestellt, das dann zu Oxalacetat umgewandelt wird, sodass der Zyklus von neuem beginnen kann. Bei diesem letzten Schritt wird noch einmal unter Verwendung des Enzyms Malat-Dehydrogenase NAD+ zu NADH + H+ reduziert.
2 Acetyl-CoA + 6 NAD+ + 2 FAD + 6 H2O + 2 ADP +2 P +2 H+ → 4 CO2 + 6 NADH + 6 H+ + 2 FADH2 + 2 CoA-SH + 2 ATP
Durch die direkte oder indirekte Verbindung mit anderen Stoffwechselwegen können auch Fettsäuren und Aminosäuren in den Citrat-Zyklus eingeschleust werden. Dabei gelangen Fettsäuren durch Acetyl-CoA in den Zyklus und Aminosäuren an verschiedenen Stellen, weiterhin können AS auch durch Umwandlungen aus Zwischenstufen des Tricarbonzykluses hergestellt werden.
Am Ende des Citrat-Zykluses sind die 6 C-Atome und die O2 -Atome der Glucose vollständig zu CO2 abgebaut worden. Zu der in der Glykolyse gewonnenen Energie in Form von ATP und NADH + H+ mit einem Betrag von 197 kJ/mol kommt nun die Energie von 2 ATP mit je 30,5 kJ/mol hinzu. Die restliche Energie des Energiegehalts der Glucose von 2836 kJ/mol liegt in dem an den Elektronenüberträgern (NADH + H+ , FADH2) gebundenen Wasserstoff.
