Chemie
- Details
- Zugriffe: 47115
Name:
Raphael Kress, 2016-12
Nomenklatur und Benennung von organischen Kohlenwasserstoffen
Allgemeines zur Genfer Nomenklatur:
Unter Nomenklatur versteht man die Benennung von Verbindungen in der Chemie. Die Regeln dieser Benennung, bestimmte die International Union of Pure and Applied Chemistry (IUPAC), um besser international zu arbeiten.
Für organische Kohlenwasserstoffe haben sich folgende Regeln ergeben:

1.Schritt: Bestimmen der längsten Kette aus Kohlenstoffatomen
Ermittle die längste Kette an Kohlenstoffatomen. Die Anzahl dieser bestimmt den Hauptkettenname.
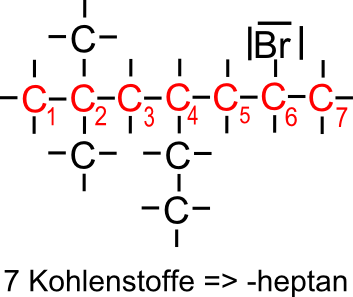
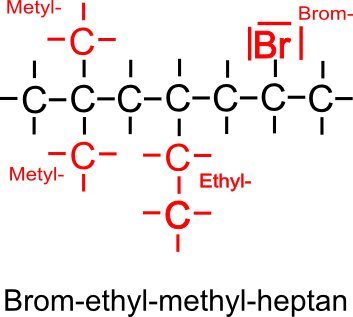
2.Schritt: Benennung der Seitenketten
Die Seitenketten werden allgemein nach Anzahl der Kohlenstoffatome ermittelt. Dabei erhalten sie die Endung "-yl", statt normalen Endung "an". Auch andere funktionelle Gruppen werden ermittelt und benannt.
Vorsilben (Präfixe) einiger funktioneller Gruppen:
- Carbonsäuren: Carboxy-
- Ester: Alkoxycarbonyl-
- Aldehyde: Formyl-
- Ketone: Oxo-
- Alkohole & Phenole: Hydroxy-
- Phenole: Hydroxy-
- Amine: Amino-
- Ether: <Gruppe>oxy-
- Alkene: <Gruppe>enyl-
- Alkine: <Gruppe>inyl-
- Halogenverbindungen: Halogen- (Bsp: 1-Brompentan)
- Alkane: <Gruppe>yl
Nachsilben (Suffixe) einiger funktioneller Gruppen:
- Carbonsäuren: <Name des Alkans/Alkens/Alkins> + säure
Beispiel: Propensäure - Ester: <Name des Alkans/Alkens/Alkins>säure
Beispiel: Carbonsäureester - Aldehyde: <Name des Alkans/Alkens/Alkins>al
Beispiel: Methanal - Ketone: <Name des Alkans/Alkens/Alkins>on
Beispiel: Decan-3-al - Alkohole & Phenole: -<Stamm>ol (alter Name: <Name des Alkans/Alkens/Alkins>ylalkohol)
Beispiel: Methanol (alter Name: Methylalkohol) - Amine: <Name des Alkans>ylamin
Beispiel: 3,5-Dimethylamin - Ether: <Name des Alkans>yl -<Name des Alkans>ylether
Beispiel: Dimethylether - Alkene: Name des Alkens
Beispiel: Prop-2-en - Alkine: Name des Alkins
Beispiel: Hept-5-in - Alkane: Name des Alkans
Beispiel: Ethan
Prioritätenliste bei der Nomenklatur organischer Verbindungen
Priorität nimmt von oben nach unten ab:
- Carbonsäuren
- Ester
- Aldehyde
- Ketone
- Alkohole
- Phenole
- Amine
- Ether
- Alkene
- Alkine
- Halogenverbindungen
- Alkane
3.Schritt: Bestimmung der Anzahl gleicher Seitenketten
Nun zählt man gleiche Seitenketten und setzt das entsprechende griechische Zahlwort vor den jeweiligen Seitenkettennamen.
Die wichtigsten griechischen Zahlwörter:
1 mono- oder hen-
2 di
3 tri
4 tetra
5 penta
6 hexa
7 hepta
8 octa
9 nona
10 deca

4.Schritt: Ermittlung der Verknüpfungsstellen
Man nummeriert die Hauptkette so durch, dass die Verknüpfungsstellen einen kleinstmögliche Zahl erhalten.

5.Schritt: FINALVERSION

Wichtiges zur Nomenklatur:
- Nach und vor jeder Zahl kommt ein Bindestrich (3,4-Dimethylpropan)
- Der erste Buchstabe des zu benennenden Stoffes wird großgeschrieben (3,4-Dimethylpropan)
- Die funktionelle Gruppe, welche die höchste Priorität besitzt, erhält den Platz des Suffixes (siehe Beispiel)
- Organische Chemie: Nukleophile Addition
- Organische Chemie: Nukleophile Substitution
- Organische Chemie: Optische Aktivität
- Organische Chemie: Oxidation und Reduktion von Aldehyden
- Organische Chemie: Oxidation von Alkoholen
- Organische Chemie: Oxidation von Glucose mit Methylenblau (blaues Wunder)
- Organische Chemie: Pektine
- Organische Chemie: Petrochemie
- Organische Chemie: Plexiglas als Kunststoff
- Organische Chemie: Polare und apolare Lösungsmittel und Lösungmitteleigenschaften (!)
- Organische Chemie: Polykondensation von Nylon
- Organische Chemie: Polysaccharide
- Organische Chemie: Propan
- Organische Chemie: Radikalische Substitution
- Organische Chemie: Reaktionsmechanismen der organischen Chemie (Übersicht)
- Organische Chemie: Redoxreaktionen und Oxidationszahlen bei organischen Verbindungen
- Organische Chemie: Saccharose
- Organische Chemie: Schmelz- und Siedebereiche von Fetten und Ölen
- Organische Chemie: Schmelz- und Siedepunkte von Alkanen und Alkenen
- Organische Chemie: Schmerzmittel
- Organische Chemie: Spiegelbildisomerie (Stereoisomerie)
- Organische Chemie: Stärke (Amylose und Amylopektin)
- Organische Chemie: Struktur- und Eigenschaftsbeziehungen bei organischen Kohlenwasserstoffen
- Organische Chemie: Tenside
- Organische Chemie: Titration von Glycin
- Organische Chemie: Typen von Carbonsäuren
- Organische Chemie: Verbrennung von Alkanen und CO2-Emission
- Organische Chemie: Vergleich von Siedepunkten bei Alkanen, Alkanolen, Aldehyden und Carbonsäuren
- Organische Chemie: Verseifung
- Organische Chemie: Viskosität
- Organische Chemie: Was ist Organische Chemie?
- Organische Chemie: Zusammensetzung von Waschmitteln
- Organische Chemie: Zusammensetzung von Waschmitteln und deren Funktion
- Organische Chemie: Zwischenmolekulare Kräfte und Anziehungskräfte zwischen Molekülen
- Physikalische Chemie: Autokatalyse
- Physikalische Chemie: Die Grundlagen der Thermodynamik
