Chemie
- Details
- Zugriffe: 38972
Name: Daniel Garrett, Niklas Jüngling, Nina & Franzi
Allgemeines zu flüssigen Alkanen
Alkane bis hin zu ca. 14-16 Kohlenstoffe liegen bei Raumtemperatur als Flüssigkeiten vor. Exemplarisch handelt dieser Artikel von den Stoffen Pentan bis Oktan.
Eigenschaften flüssiger Alkane
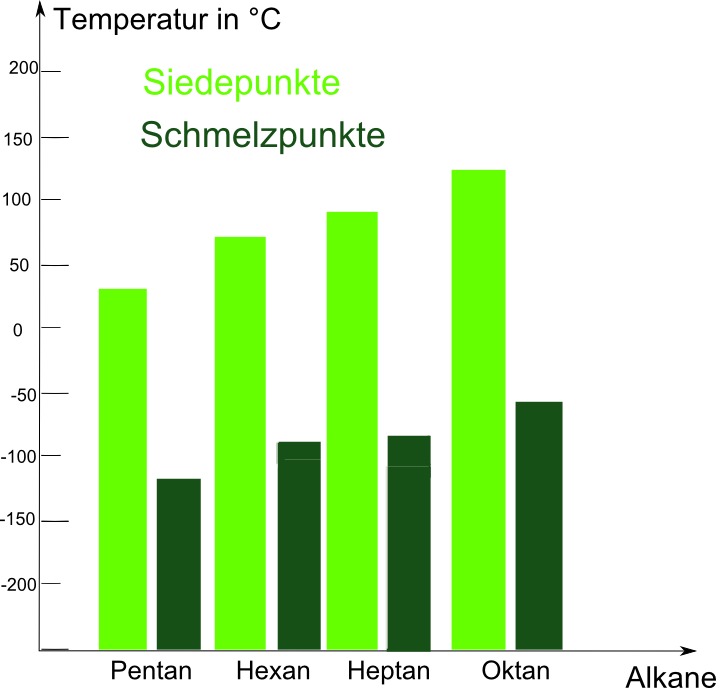
- durch größere Oberfläche => höherer Schmelz-/Siedepunkt
- flüssige Alkane: 5-16 C-Atome => Sdp: 35 - 140°C
- Nichtleiter
- schlecht wasserlöslich
- leicht entzündlich
- geringe Reaktivität (weil C-Bindungen sehr stabil sind)
=> Bsp.: Erdöl seit Jahrmillionen chemisch unverändert
Vorkommen flüssiger Alkane
- Erdöl
- im Sonnensystem fast überall (Meteoriten, Gasplaneten wie z. B. Jupiter,...)
- auf der Erde oft als Spurenelement
Verwendung flüssiger Alkane:
- Pentan: Kältemittel in Kühlschränken und Klimaanlagen
- Hexan: Verdünnungsmittel für Lacke und Klebstoffe, Herstellung von Kunststoffen
- Heptan: Lösungsmittel in der organischen Synthese
- Oktan: Lösungs- und Reinigungsmittel, enthalten in Flugzeug- und Autobenzin
- Nonan/Neptan: Bestandteil von Kraftstoffen
- Dekan: Bestandteil von Kraftstoffen
Reaktionen flüssiger Alkane:
Verbrennung von Oktan:
vollständige Verbrennung:
2 C8H18 + 25 O2 --->16 CO2 + 18 H2O
Unvollständige Verbrennung:
2 C8H18 + 6 O2 ---> 6 C + CO + CO2 + 9 H2O
Ein Video zur Verbennung einiger Alkane: Chemieversuche: Verbrennung & Oxidation von Alkanen (Oktan, Heptan, Pentan) sowie Ethanol
Flüssige Alkane im Detail:
Pentan:
Eigenschaften von Pentan:
- Summenformel ~ C5H12
- farblose Flüssigkeit ( Im Normalzustand)
- benzinartig riechend
- Smp -130° ; Sdp 36° (Der niedrige Siedepunkt kann zu Nebenwirkungen ( Kopfschmerzen,..) bei menschen führen)
- 3 Isomere (n-Pentan; iso-Pentan; neo-Pentan)
Vorkommen und Gewinnung von Pentan:
Pentan kommt im Erdöl vor. Sie können durch Destillation aus Erdgasen, Crackgasen(Gase, bei denen längere Kettenlängen in kürzere Kettenlängen gespaltet werden) und Benzinen gewonnen werden.
Verwendung vonPentan:
Es wird sowohl als Kältemittel in Kühlschränken und Klimaanlangen verwendet, als auch zum Schäumen von Polyurethan-Hartschäumen. Diese sind uns auch als Schaumgummi bekannt, die zum Beispiel zum Abdämmen der Kälte unter Dächern befestigt werden.
Reaktionen von Pentan:
Bsp: Radikalische Subsitution
C5H12 + Cl2 -> C5H11Cl + HCl
Hexan:
Eigenschaften von Hexan:
-Summenformel ~C6H14
-farblose Flüssigkeit
-5 Isomere
-Schmelzpunkt: -95°C ; Siedepunkt: 69°C
-Benzingeruch
- leicht entzündlich
Vorkommen/Gewinnung von Hexan:
Hexan wird überweigend aus Erdöl gewonnen.
Verwendung von Hexan:
Hexan wird hauptsächlich als Lösungsmittel, Schmieröl und Heizöl verwendet. Als Lösungsmittel wird es besonders als Lösungsmittel für Polystrol, einem Kunststoff in Styropor, verwendet.
Reaktionen von Hexan:
Bromierung:
C6H14 + Br2 -> C6H13Br + HBr
Heptan:
Eigenschaften von Heptan:
-Summenformel ~ C7H16
- farblose Flüssigkeit (Im Normalzustand)
- SMP -91° ; SDP 98°
- 9 Isomere
Vorkommen/Gewinnung von Heptan:
Heptan wird aus Erdöl gewonnen. Des Weiteren kann man es auch aus ätherischen Ölen einiger Kiefern gewinnen. Ebenso die Petroleumnüsse auf den Philippinen dienen zur Gewinnung von Heptan.
Verwendung von Heptan:
Heptan dient als Lösungs- und Extraktionsmittel(Substanz die Komponenten aus einem Gemisch löst).
Oktan:
Eigenschaften von Oktan:
- Summenformel ~C8H18
- farblose Flüssigkeit
- Schmelzpunkt:-56.8°C ; Siedepunkt: 126°C
- 18 Isomere
- Benzingeruch
Vorkommen/ Gewinnung von Oktan:
Oktan kommt in Erdöl vor.
Verwendung von Oktan:
- Organische Chemie: Alkane - gasförmige Alkane
- Organische Chemie: Alkanole (Alkohole)
- Organische Chemie: Alkene und Alkine
- Organische Chemie: Alkohol und seine Wirkung auf Menschen
- Organische Chemie: Alkoholate
- Organische Chemie: Alkohole: Ethanolherstellung durch alkoholische Gärung und großtechnische Produktion
- Organische Chemie: Aminosäuren - Peptidbindung, Typen, Aufbau, Reaktionen
- Organische Chemie: Anorganische Ester
- Organische Chemie: Aufgaben und Übungen zur Nomenklatur bei organischen Verbindungen
- Organische Chemie: Benzin und Diesel
- Organische Chemie: Bestimmung von Schmelz- und Siedepunkten
- Organische Chemie: Biogasanlagen
- Organische Chemie: Brennbarkeit von Kohlenwasserstoffen
- Organische Chemie: Carbonsäuren: homologe Reihe, Verwendung
- Organische Chemie: Carbonylverbindungen - Aldehyde
- Organische Chemie: Carbonylverbindungen - Ketone
- Organische Chemie: chemische Nachweise bei organischen Verbindungen
- Organische Chemie: Cis-/ trans-Isomerie und E/Z-Isomerie
- Organische Chemie: Cycloalkane und Cykloalkene
- Organische Chemie: Darstellungsweisen organischer Verbindungen
- Organische Chemie: Der Einfluss der I-Effekte auf die Säurestärke
- Organische Chemie: Diamanten und Edelsteine im Vergleich
- Organische Chemie: Die Aminosäure Glycin
- Organische Chemie: Die Chemie der "Shisha"
- Organische Chemie: Die Harnstoffsynthese von Friedrich Wöhler
- Organische Chemie: Eigenschaften von Aminosäuren
- Organische Chemie: Einfluss von Molekülmasse und Van der Waals-Kräften auf die Schmelz- und Siedepunkte
- Organische Chemie: Elektrophile und nukleophile Addition
- Organische Chemie: Eliminierung
- Organische Chemie: Energetische Betrachtung organischer Reaktionen
- Organische Chemie: Erdöl und Erdgas
- Organische Chemie: Erdöldestillation zur Gewinnung von Kohlenwasserstoffen
- Organische Chemie: Ester und die Veresterung
- Organische Chemie: Esterspaltung durch Hydrolyse
- Organische Chemie: Ethan
- Organische Chemie: Ethanol
- Organische Chemie: Ethen, Propen und Buten
- Organische Chemie: Ethin
- Organische Chemie: Ethin, Propin, Butin
- Organische Chemie: Färbeverfahren
- Organische Chemie: Fehlingprobe & Tollens-Probe
- Organische Chemie: Fehlingprobe und reduzierende Eigenschaften bei Kohlenhydraten
- Organische Chemie: Fette
- Organische Chemie: Fetthärtung und Margarineherstellung
- Organische Chemie: Fettsäuren
- Organische Chemie: Fischer-Projektion und die Umwandlung in die Haworth-Projektion
- Organische Chemie: Fluor-Chlor-Kohlenwasserstoffe (FCKW)
- Organische Chemie: Fruchtsäuren
- Organische Chemie: Fructose
- Organische Chemie: Galactose (!)
- Organische Chemie: Glucose (Traubenzucker)
- Organische Chemie: Glycogen (tierische Stärke)
- Organische Chemie: Glycosidische Bindung
- Organische Chemie: Gummi und Kautschuk
- Organische Chemie: Halogenalkane (!)
- Organische Chemie: Homologe Reihe der Alkane (!)
- Organische Chemie: I-Effekte
- Organische Chemie: Insulin
- Organische Chemie: Isobuten
- Organische Chemie: Isomaltose & Maltose als typische Disaccharide
- Organische Chemie: Isomerieformen
- Organische Chemie: Kerosin und Schweröl als Erdölbestandteile
- Organische Chemie: Keto-En(di)ol-Tautomerie bei Monosacchariden
- Organische Chemie: Kohle und Graphit
- Organische Chemie: Kohlenhydrate - Disaccharide
- Organische Chemie: Kunststoffe I - Allgemeines und radikalische Polymerisation
- Organische Chemie: Kunststoffe im Vergleich: Thermoplaste
- Organische Chemie: Lactose
- organische Chemie: Löslichkeit von organischen Verbindungen (polare und apolare Lösungsmittel)
- Organische Chemie: Mechanismus Veresterung
- Organische Chemie: mehrwertige Alkohole (Alkanole)
- Organische Chemie: Methan
- Organische Chemie: Nachweis von Proteinen (Ninhydrin-Reaktion)
- Organische Chemie: Nachweise für ungesättige Fettsäuren
- Organische Chemie: Nitril als wichtiger Kunststoff
- Organische Chemie: Nomenklatur und Benennung von organischen Kohlenwasserstoffen
- Organische Chemie: Nukleophile Addition
- Organische Chemie: Nukleophile Substitution
- Organische Chemie: Optische Aktivität
- Organische Chemie: Oxidation und Reduktion von Aldehyden
- Organische Chemie: Oxidation von Alkoholen
- Organische Chemie: Oxidation von Glucose mit Methylenblau (blaues Wunder)
- Organische Chemie: Pektine
- Organische Chemie: Petrochemie
- Organische Chemie: Plexiglas als Kunststoff
- Organische Chemie: Polare und apolare Lösungsmittel und Lösungmitteleigenschaften (!)
- Organische Chemie: Polykondensation von Nylon
- Organische Chemie: Polysaccharide
- Organische Chemie: Propan
- Organische Chemie: Radikalische Substitution
- Organische Chemie: Reaktionsmechanismen der organischen Chemie (Übersicht)
- Organische Chemie: Redoxreaktionen und Oxidationszahlen bei organischen Verbindungen
- Organische Chemie: Saccharose
- Organische Chemie: Schmelz- und Siedebereiche von Fetten und Ölen
- Organische Chemie: Schmelz- und Siedepunkte von Alkanen und Alkenen
- Organische Chemie: Schmerzmittel
- Organische Chemie: Spiegelbildisomerie (Stereoisomerie)
- Organische Chemie: Stärke (Amylose und Amylopektin)
- Organische Chemie: Struktur- und Eigenschaftsbeziehungen bei organischen Kohlenwasserstoffen
- Organische Chemie: Tenside
- Organische Chemie: Titration von Glycin
- Organische Chemie: Typen von Carbonsäuren
- Organische Chemie: Verbrennung von Alkanen und CO2-Emission
- Organische Chemie: Vergleich von Siedepunkten bei Alkanen, Alkanolen, Aldehyden und Carbonsäuren
- Organische Chemie: Verseifung
- Organische Chemie: Viskosität
- Organische Chemie: Was ist Organische Chemie?
- Organische Chemie: Zusammensetzung von Waschmitteln
- Organische Chemie: Zusammensetzung von Waschmitteln und deren Funktion
- Organische Chemie: Zwischenmolekulare Kräfte und Anziehungskräfte zwischen Molekülen
- Physikalische Chemie: Autokatalyse
- Physikalische Chemie: Die Grundlagen der Thermodynamik
