Chemie
- Details
- Zugriffe: 11597
Name: Raphael Kress, 2018-04
Name: Umed Danesch, Furkan Oktay 2019-11
Photovoltaik und Brennstoffzelle
Allgemeines zur Brennstoffzelle
Im Vergleich zu Wärmekraftwerken, welche einen Wirkungsgrad von ca. 40% besitzen, sind Stromerzeuger, welche auf galvanischen Zellen basieren, die einen Wirkungsgrad von bis zu 80% erreichen können, viel effektiver. Der Wirkungsgrad gibt dabei das Verhältnis von gewonnener zu aufgewendeter Energie an.
Die bei einer Redoxreaktion frei werdende Energie wird bei der galvanischen Zelle direkt in elektrische Energie umgewandelt. Dabei muss bei einer galvanischen Zelle der Brennstoff dauerhaft nachgeführt werden um über einen längeren Zeitraum Energie erzeugen zu können.
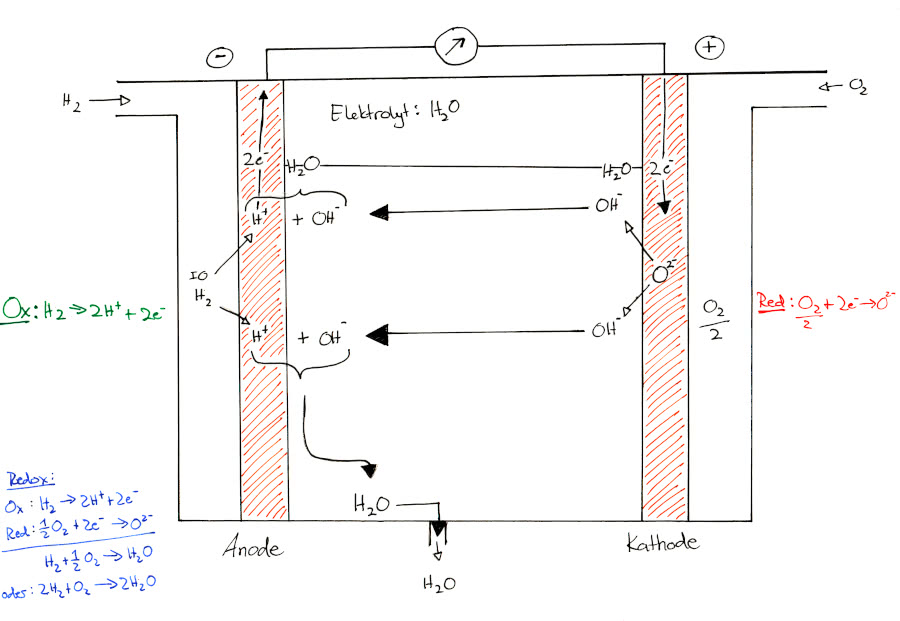
Aufbau der Brennstoffzelle:
siehe: https://commons.wikimedia.org/wiki/File:Brennstoffzelle_funktionsprinzip.png
Die Brennstoffzelle besteht zunächst aus zwei Elektroden, meist aus Metall oder Kohlenstoff. Diese sind mit einem Katalysator, zum Beispiel Platin beschichtet. Die beiden Elektroden sind durch eine/n Elektrolytmembran/Elektrolyten voneinander getrennt. Diese ist nur für eine bestimmte Ionensorte durchlässig. Meist werden Laugen oder Säuren als Elektrolyten verwendet.
Chemische Funktionsweise einer Brennstoffzelle
In einer Wasserstoff/Sauerstoff-Brennstoffzelle wird die bei der stark exotherm ablaufenden Oxidation freiwerdende Energie genutzt:
2 H2 (g) + O2 (g) ----> 2 H2O (l)
Eine beispielhafte Brennstoffzelle ist die Protonenaustauschmembran-Brennstoffzelle (PEMFC), bei welcher Wasserstoff an der Anode katalytisch zu Protonen oxidiert wird, und Elektronen abgegeben werden. Über die Ionen-Membran gelangen die Protonen zur Kammer der Kathode. Die Elektronen hingegen gelangen über einen elektrischen Leiter und schließlich einen elektrischen Verbraucher zur Kathode, wo sie mit den ankommenden Protonen und zugeführtem Luftsauerstoff wieder zu Wasser reagieren (siehe Reaktion oben). Da die Membran in diesem Fall nur für Protonen durchlässig ist, spricht man von einem sauren Elektolyten.
Chemische Reaktionen der Brennstoffzelle (Redoxreaktionen)
Brennstoffzelle mit saurem Elektrolyten
Anode: Minuspol: 2 H2 (g) + 4 H2O(l) ----> 4 H3O+ (aq) + 4e- U=-0,87V
Kathode: Pluspol: O2 (g) + 4 H3O+ (aq) + 4e- ----> 6 H2O (l) U=0,36V
----------------------------------------------------------------------------------------
Gesamtreaktion: 2 H2 (g) + O2 (g) ----> 2 H2O (l) U=1,23V
Brennstoffzelle mit basischem Elektrolyten
Gleiches gilt für einen basischen Elektrolyten, welche aber mit hochreinem Sauerstoff und Wasserstoff arbeiten:
Anode: Minuspol: 2 H2 (g) + 4 OH-(aq) ----> 4 H2O (aq) + 4e- U=-0,87V
Kathode: Pluspol: O2 (g) + H2O (aq) + 4e- ----> 4 OH-(aq) U=0,36V
----------------------------------------------------------------------------------------
Gesamtreaktion: 2 H2 (g) + O2 (g) ----> 2 H2O (l) U=1,23V
Aus den Redoxreaktionen ergibt sich eine theoretische Spannung von 1,23 V, welche bei Standardbedingungen (25°C) erreicht werden könnte. Im Betrieb werden meist jedoch nur Spannungen von 0,5 V bis 1 V erreicht. Dabei ist die erzeugte Spannung von der Temperatur und der Qualität der Zelle abhängig. Um größere Spannungen zu erzeugen, werden oft mehrere Zellen zu einem "stack" in Reihe geschaltet.
Verwendung
Aufgrund der Vorteile wie zum Beispiel einem guten Wirkungsgrad, Klimafreundlichkeit und Herstellung elektrischer Energie, ohne viel Wärmeenergie zu erzeugen, bietet die Brennstoffzelle folgende Anwendungen:
1) Raketenantriebe
2) Schiffsantriebe
3) Unterwasserbootantriebe
4) Fahrzeuge mit Brennstoffzellen
Photovoltaik
Allgemeines
Photovoltaikanlagen erzeugen ebenfalls elektrischen Strom. Dieser Prozess basiert auf der Fähigkeit mancher Stoffe, Licht direkt in Strom umzuwandeln.
Aufbau und Funktionsweise
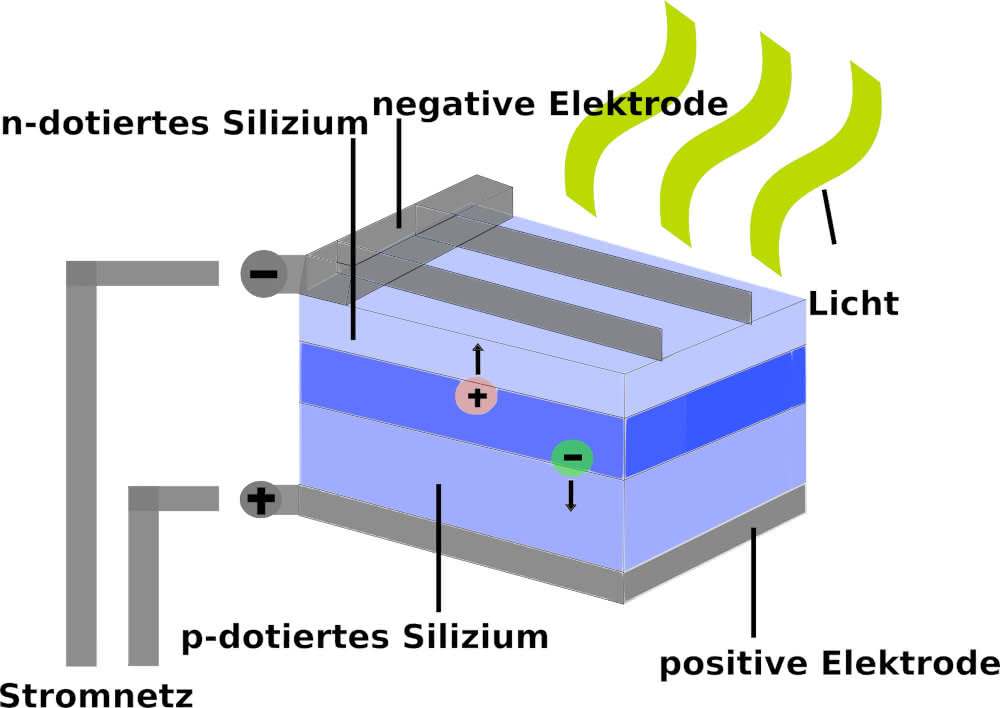
Die meisten Solarzellen basieren heutzutage auf Silizium, welches ein Halbleiter ist. Als Halbleiter bezeichnet man jene Stoffe, die sich sowohl wie ein elektrischer Leiter, als auch wie ein Nichtleiter verhalten, können. Das nicht leitende Material in der Solarzelle wird durch Absorption ("Aufnahme") eines Photons ("Lichtteilchen") zu einem Leiter, indem die Lichtenergie des Photons die Elektronen aus dem Kristallverbund lösen. Der erzeugte Strom besteht dann schließlich aus den sich bewegenden Elektronen. Die Photonenenergie, welche durch die Frequenz des Lichts charakterisiert ist, muss in einem gewissen vom Material abhängigen Bereich liegen. Daher können auch nur bestimmte Lichtfrequenzen für die Stromerzeugung genutzt werden.
Dotierung
Die Dotierung bezeichnet das Einfügen von Fremdatomen in eine Schicht eines Schaltkreises beziehungsweise eines Halbleiters. Bei der p-Dotierung werden Fremdatome in den Halbleiter implantiert, welche als Elektronen-Akzeptoren fungieren, während bei der n-Dotierung Elektronen-Donatoren implantiert werden.
Forschung
Die Forschung im Bereich der Photovoltaiktechnik ist trotz der Tatsache, dass das Phänomen bereits lange bekannt ist, noch lange nicht zu Ende. Es wird nach einem neuen Material gesucht, welches Silizium ersetzen kann. Dieses soll ein großen Teil des Lichtspektrums nutzbar machen und eine geringe Rekombinationsrate besitzen. Die Rekombinationsrate gibt an, wie schnell die Elektronen von einem leitenden in einen nicht leitenden Zustand wechseln. Der geringe Wirkungsgrad heutiger Solarzellen kommt deren hoher Rekombinationsrate zu Schulden.
- Anorganische Chemie: Protolyse von Phosphorsäure
- Anorganische Chemie: Protolysereaktionen bei Salzen (Säure-Base Reaktionen)
- Anorganische Chemie: Reaktion von Säuren und Basen mit Wasser
- Anorganische Chemie: Reaktionsgeschwindigkeit und Messung der Reaktionsgeschwindigkeit
- Anorganische Chemie: Reaktionsgeschwindigkeit, Momentangeschwindigkeit und Messung (sowie HWZ)
- Anorganische Chemie: Reaktionsgeschwindigkeitsmessung von Thiosulfationen mit Säure
- Anorganische Chemie: Redoxreaktionen aufstellen
- Anorganische Chemie: Redoxreaktionen im Alltag
- Anorganische Chemie: Salpetersäure HNO₃ - Herstellung, Verwendung, Eigenschaften
- Anorganische Chemie: Salpetrige Säure
- Anorganische Chemie: Salze
- Anorganische Chemie: Salzherstellung durch Neutralisation
- Anorganische Chemie: Sauerstoff
- Anorganische Chemie: Sauerstoffsäuren des Chlors
- Anorganische Chemie: Sauerstoffsäuren des Phosphors
- Anorganische Chemie: Säure-Base Chemie (Brönsted-Definitionen)
- Anorganische Chemie: Säure-Base-Puffer und Puffersysteme
- Anorganische Chemie: Säurestärke (pKs) und Basenstärke (pKb)
- Anorganische Chemie: Schwefel
- Anorganische Chemie: Schwefelsäure
- Anorganische Chemie: Stickstoff
- Anorganische Chemie: Struktur von Salzen, Ionengitter und Ionenbildung
- Anorganische Chemie: Übungsaugaben zum Massenwirkungsgesetz (MWG)
- Anorganische Chemie: Vergleich von Ionenbindung und Atombindung
- Anorganische Chemie: Wasserstoff
- Anorganische Chemie: Wie berechnet man Neutralistionsaufgaben (Beispielaufgaben)
- Anorganische Chemie: Wie funktioniert der Lithium-Ionen-Akku?
- Anorganische Chemie: Zink
- Anorgansiche Chemie: Redoxreaktion - Beispielaufgaben
- Biochemie: Biokatalysatoren (Enzyme)
- Chemie: Oxidationszahlen und deren Bestimmung (!)
- Farbigkeit und Molekülstruktur
- Glossar: Fachbegriffe der anorganischen und organischen Chemie mit Erklärungen
- Komplexchemie: Anwendungen der Komplexchemie
- Komplexchemie: Aquakomplexe
- Komplexchemie: Aufbau von Komplexen
- Komplexchemie: Chelatkomplexe
- Komplexchemie: Historischer Abriss der Entdeckung der Komplexchemie
- Komplexchemie: In der Natur vorkommende (biologische) Komplexverbindungen
- Komplexchemie: Komplexe Gleichgewichtsreaktionen und die Stabilitätskonstanten
- Komplexchemie: Komplexstabilitätskonstante und Komplexzerfallskonstante
- Komplexchemie: Ligandenaustauschreaktionen
- Komplexchemie: Nomenklatur (Benennung) von Komplexen
- Komplexchemie: Wasserenthärtung
- Ökologische, ökonomische und soziale Nachhaltigkeit in Chemie
- Organische Chemie: Gelatine
- Selektivität und Spezifität von Katalysatoren
- Herstellung von Maßlösungen
- I-Effekte beeinflussen die Säurestarke von Carbonsäuren
- Organische Chemie: Oxidative Fettumwandlung (Ranzigwerden von Fetten)
- Organische Chemie: Alkane - feste Alkane // Wachse und Paraffine
- Organische Chemie: Alkane - flüssige Alkane
- Organische Chemie: Alkane - gasförmige Alkane
- Organische Chemie: Alkanole (Alkohole)
- Organische Chemie: Alkene und Alkine
- Organische Chemie: Alkohol und seine Wirkung auf Menschen
- Organische Chemie: Alkoholate
- Organische Chemie: Alkohole: Ethanolherstellung durch alkoholische Gärung und großtechnische Produktion
- Organische Chemie: Aminosäuren - Peptidbindung, Typen, Aufbau, Reaktionen
- Organische Chemie: Anorganische Ester
- Organische Chemie: Aufgaben und Übungen zur Nomenklatur bei organischen Verbindungen
- Organische Chemie: Benzin und Diesel
- Organische Chemie: Bestimmung von Schmelz- und Siedepunkten
- Organische Chemie: Biogasanlagen
- Organische Chemie: Brennbarkeit von Kohlenwasserstoffen
- Organische Chemie: Carbonsäuren: homologe Reihe, Verwendung
- Organische Chemie: Carbonylverbindungen - Aldehyde
- Organische Chemie: Carbonylverbindungen - Ketone
- Organische Chemie: chemische Nachweise bei organischen Verbindungen
- Organische Chemie: Cis-/ trans-Isomerie und E/Z-Isomerie
- Organische Chemie: Cycloalkane und Cykloalkene
- Organische Chemie: Darstellungsweisen organischer Verbindungen
- Organische Chemie: Der Einfluss der I-Effekte auf die Säurestärke
- Organische Chemie: Die Aminosäure Glycin
- Organische Chemie: Die Chemie der "Shisha"
- Organische Chemie: Die Harnstoffsynthese von Friedrich Wöhler
- Organische Chemie: Eigenschaften von Aminosäuren
- Organische Chemie: Einfluss von Molekülmasse und Van der Waals-Kräften auf die Schmelz- und Siedepunkte
- Organische Chemie: Elektrophile und nukleophile Addition
- Organische Chemie: Eliminierung
- Organische Chemie: Energetische Betrachtung organischer Reaktionen
- Organische Chemie: Erdöl und Erdgas
- Organische Chemie: Erdöldestillation zur Gewinnung von Kohlenwasserstoffen
- Organische Chemie: Ester und die Veresterung
- Organische Chemie: Esterspaltung durch Hydrolyse
- Organische Chemie: Ethan
- Organische Chemie: Ethanol
- Organische Chemie: Ethen, Propen und Buten
- Organische Chemie: Ethin
- Organische Chemie: Ethin, Propin, Butin
- Organische Chemie: Färbeverfahren
- Organische Chemie: Fehlingprobe & Tollens-Probe
- Organische Chemie: Fehlingprobe und reduzierende Eigenschaften bei Kohlenhydraten
- Organische Chemie: Fette
- Organische Chemie: Fetthärtung und Margarineherstellung
- Organische Chemie: Fettsäuren
- Organische Chemie: Fischer-Projektion und die Umwandlung in die Haworth-Projektion
- Organische Chemie: Fluor-Chlor-Kohlenwasserstoffe (FCKW)
- Organische Chemie: Fruchtsäuren
- Organische Chemie: Fructose
- Organische Chemie: Galactose (!)
- Organische Chemie: Glucose (Traubenzucker)
- Organische Chemie: Glycogen (tierische Stärke)
- Organische Chemie: Glycosidische Bindung
- Organische Chemie: Gummi und Kautschuk
- Organische Chemie: Halogenalkane (!)
- Organische Chemie: Homologe Reihe der Alkane (!)
- Organische Chemie: I-Effekte
- Organische Chemie: Insulin
- Organische Chemie: Isobuten
- Organische Chemie: Isomaltose & Maltose als typische Disaccharide
- Organische Chemie: Isomerieformen
- Organische Chemie: Kerosin und Schweröl als Erdölbestandteile
- Organische Chemie: Keto-En(di)ol-Tautomerie bei Monosacchariden
- Organische Chemie: Kohle und Graphit
- Organische Chemie: Kohlenhydrate - Disaccharide
- Organische Chemie: Kunststoffe I - Allgemeines und radikalische Polymerisation
- Organische Chemie: Kunststoffe im Vergleich: Thermoplaste
- Organische Chemie: Lactose
- organische Chemie: Löslichkeit von organischen Verbindungen (polare und apolare Lösungsmittel)
- Organische Chemie: Mechanismus Veresterung
- Organische Chemie: mehrwertige Alkohole (Alkanole)
- Organische Chemie: Methan
- Organische Chemie: Nachweis von Proteinen (Ninhydrin-Reaktion)
- Organische Chemie: Nachweise für ungesättige Fettsäuren
- Organische Chemie: Nitril als wichtiger Kunststoff
- Organische Chemie: Nomenklatur und Benennung von organischen Kohlenwasserstoffen
- Organische Chemie: Nukleophile Addition
- Organische Chemie: Nukleophile Substitution
- Organische Chemie: Optische Aktivität
- Organische Chemie: Oxidation und Reduktion von Aldehyden
- Organische Chemie: Oxidation von Alkoholen
- Organische Chemie: Oxidation von Glucose mit Methylenblau (blaues Wunder)
- Organische Chemie: Pektine
- Organische Chemie: Petrochemie
- Organische Chemie: Plexiglas als Kunststoff
- Organische Chemie: Polare und apolare Lösungsmittel und Lösungmitteleigenschaften (!)
- Organische Chemie: Polykondensation von Nylon
- Organische Chemie: Polysaccharide
- Organische Chemie: Propan
- Organische Chemie: Radikalische Substitution
- Organische Chemie: Reaktionsmechanismen der organischen Chemie (Übersicht)
- Organische Chemie: Redoxreaktionen und Oxidationszahlen bei organischen Verbindungen
- Organische Chemie: Saccharose
- Organische Chemie: Schmelz- und Siedebereiche von Fetten und Ölen
- Organische Chemie: Schmelz- und Siedepunkte von Alkanen und Alkenen
- Organische Chemie: Schmerzmittel
- Organische Chemie: Spiegelbildisomerie (Stereoisomerie)
- Organische Chemie: Stärke (Amylose und Amylopektin)
- Organische Chemie: Struktur- und Eigenschaftsbeziehungen bei organischen Kohlenwasserstoffen
- Organische Chemie: Tenside
- Organische Chemie: Titration von Glycin
- Organische Chemie: Typen von Carbonsäuren
- Organische Chemie: Verbrennung von Alkanen und CO2-Emission
- Organische Chemie: Vergleich von Siedepunkten bei Alkanen, Alkanolen, Aldehyden und Carbonsäuren
- Organische Chemie: Verseifung
- Organische Chemie: Viskosität
- Organische Chemie: Was ist Organische Chemie?
- Organische Chemie: Zusammensetzung von Waschmitteln
- Organische Chemie: Zusammensetzung von Waschmitteln und deren Funktion
- Organische Chemie: Zwischenmolekulare Kräfte und Anziehungskräfte zwischen Molekülen
- Physikalische Chemie: Die Grundlagen der Thermodynamik